국내에서 개발된 신약과 희귀의약품이 2배 이상 증가한 것으로 나타났다. 제약·바이오 기업 연구개발(R&D) 성과가 가시화되고 있다는 평가다.
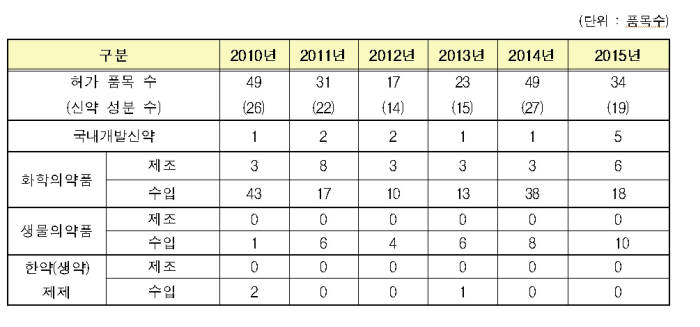
식품의약품안전처 식품의약품안전평가원은 지난해 허가·신고된 의약품 3014개 품목 중 국내 개발 신약은 2014년 1개 품목에서 지난해 5개 품목으로 증가했다. 희귀의약품 허가도 49개 품목으로 전년대비(28개 품목) 2배 가까이 증가했다.
전체 의약품 중 약효군별 허가·신고 현황을 보면 해열진통소염제 등이 포함된 신경계용 의약품이 517개 품목(18%)으로 가장 많았다. 당뇨병치료 등 대사성의약품 393개 품목(13%), 순환계용의약품 359개 품목(12%), 소화계용의약품 358개 품목(12%), 비뇨·생식기관 및 항문용약 329개 품목(11%)이 뒤를 이었다.
지난해 허가받은 신약 34개는 신경계치료제와 당뇨병치료제가 각각 8개 품목으로 가장 많았다. 항암제, 항바이러스제가 각각 5개 품목이다.
화학의약품은 신약 24개 품목, 자료제출의약품 295개 품목, 희귀의약품 38개 품목 및 원료의약품 98개 품목이 허가됐다. 생물의약품은 신약 10개 품목, 자료제출의약품 30개 품목, 희귀의약품 11개 품목, 세포치료제 1개 품목이 허가됐다.
특히 자료제출의약품은 2014년 132개 품목에서 지난해 259개 품목으로 2배 이상 증가했다. 고지혈증 복합제 등 복약 순응도를 높이기 위한 복합제 개발이 증가했기 때문이다. 자료제출의약품은 신약은 아니나 안전성·유효성 심사가 필요한 품목이다.
생물의약품은 신약 10개 품목, 자료제출의약품 30개 품목, 희귀의약품 11개 품목, 세포치료제 1개 품목이 허가됐다. 최근 개발이 활발한 유전자재조합의약품이 40개 품목으로 가장 많다. 세포배양 독감백신 등 생물학적제제와 세포치료제도 각각 11개 품목, 1개 품목 순으로 나타났다.
정용철 의료/SW 전문기자 jungyc@etnews.com









