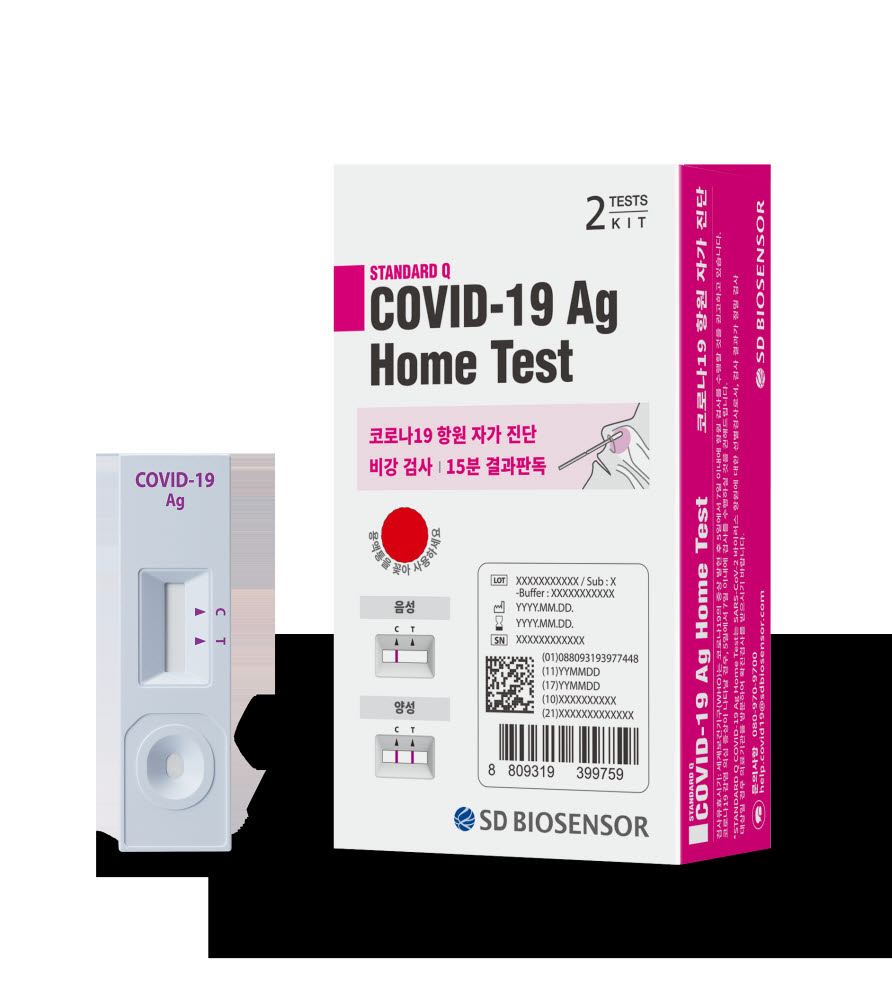
식품의약품안전처는 23일 코로나19 자가검사가 가능한 항원방식 자가검사키트 2개 제품을 조건부 허가했다.
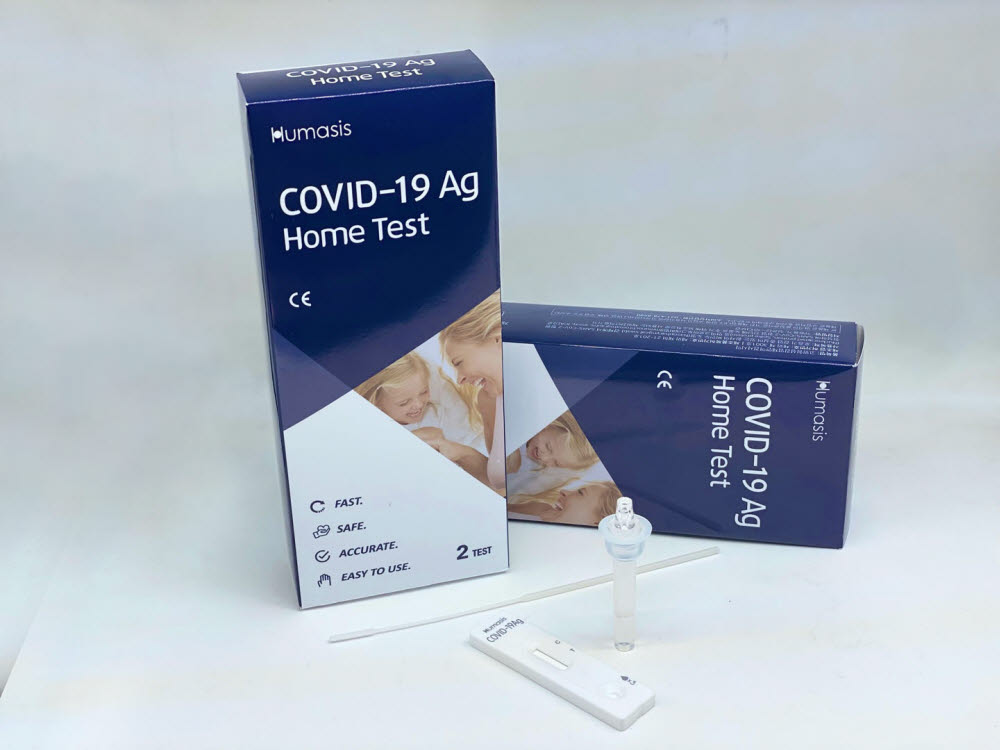
허가받은 제품은 에스디바이오센서의 'STANDARD Q COVID-19 Ag Home Test'와 휴마시스의 'Humasis COVID-19 Ag Home Test' 2종이다.
조건부 허가에 따라 정식 허가 제품이 나오기 전까지 두 제품을 국내에서 한시적으로 사용할 수 있다. 업체들은 임상적 성능시험 자료 등을 3개월 이내에 추가로 제출해야 한다. 판매는 허가 후 7~10일 이후 약국, 인터넷 등을 통해 가능할 전망이다.
이번에 허가한 코로나19 자가검사키트 두 제품은 국내에서 전문가용으로 허가를 받은 제품이고 해외에서는 자가검사용 임상시험을 실시해 긴급사용승인을 받았다.
에스디바이오센서 제품은 독일, 네덜란드, 덴마크, 스위스, 포르투칼, 룩셈부르크, 체코 등 7개국에서 자가검사용으로 사용 중이다. 독일에서 자가검사용으로 실시한 결과 임상적 민감도는 82.5%(33/40명), 특이도는 100%(105/105명)로 나타났다.
휴마시스 제품은 체코, 덴마크, 오스트리아 등 3개국에서 자가검사용으로 사용되며 체코와 브라질에서 자가검사용으로 실시한 임상적 민감도는 92.9%(52/56명), 특이도는 99.0%(95/96명)였다.
민감도는 환자를 양성으로 판정할 확률, 특이도는 환자가 아닌 사람을 음성으로 판정할 확률이다.
식약처는 “두 제품은 코로나19 확산과 대유행 우려에 따라 전문가가 아닌 개인이 손쉽게 자가검사를 할 수 있는 보조적인 수단으로 다양한 검사방법을 통해 감염 확산을 줄이기 위해 허가됐다”면서 “코로나19 감염 증상의 확진이 아닌 보조적인 수단으로만 사용해야 하며, 유전자 검사 결과와 임상증상 등을 고려해 의사가 감염 여부를 최종 판단해야 한다”고 강조했다.
두 제품 모두 자가검사용으로 코로나19 바이러스 감염 증상자의 비강 도말 검체에서 바이러스의 항원을 검출해 검사하는 방식이고 15분 내외로 결과를 확인할 수 있다.
하지만 기존 유전자 검사(PCR) 방식이나 의료인 또는 검사전문가가 콧속 깊은 비인두에서 검체를 채취하여 수행하는 항원 방식에 비해 민감도가 낮다는 단점이 있어 방역수칙을 철저히 준수함을 전제로 주의 깊게 사용돼야한다고 식약처는 설명했다.
식약처에 따르면 증상이 의심되는 경우 유전자 검사를 먼저 실시해야 하며, 유전자 검사가 어려운 경우 자가검사키트로 검사하되, 붉은색 두줄(대조선 C, 시험선 T)이 나타나는 경우 반드시 유전자 검사를 받아야 하고, 붉은색 한줄(대조선 C)이 나타나는 경우에도 감염이 의심되거나 증상이 있으면 유전자 검사를 받아야 한다.
또 사용자는 사용설명서를 충분히 숙지하고 사용방법에 따라 정확하게 사용해야 하며, 검사 결과와 무관하게 코로나19 증상이 있으면 바로 선별진료소 등을 방문해 유전자 검사를 받아야 한다.
정현정기자 iam@etnews.com









