광주과학기술원(GIST·총장 김기선)은 서지원 화학과 교수팀이 고리형 펩타이드 세포막 투과 및 경구투여 원리를 규명, 신약개발 가능성을 제시했다고 22일 밝혔다.
펩타이드 약물은 낮은 세포막 투과성과 낮은 경구투여율, 빠른 분해성 등으로 제약 시장에서 외면받아 왔다. 하지만 최근 대량 생산·서열 분석·약물 제형 기술 등이 개발되면서 약물로 승인받는 횟수가 증가하는 추세다. 펩타이드 C-말단과 N-말단을 이어붙인 고리형 펩타이드가 각광을 받고 있다. 면역억제제로 사용중인 사이클로스포린 A가 대표적이다.
서 교수팀이 발굴한 고리형 펩타이드는 사이클로스포린 A의 구조적 유사체인 사이클로스포린 O이다. 두 물질을 비교 연구해 분자량 1000 달톤(Da) 이상의 고리형 펩타이드가 경구투여 약물로 개발되기 위한 구조적 조건을 규명했다.
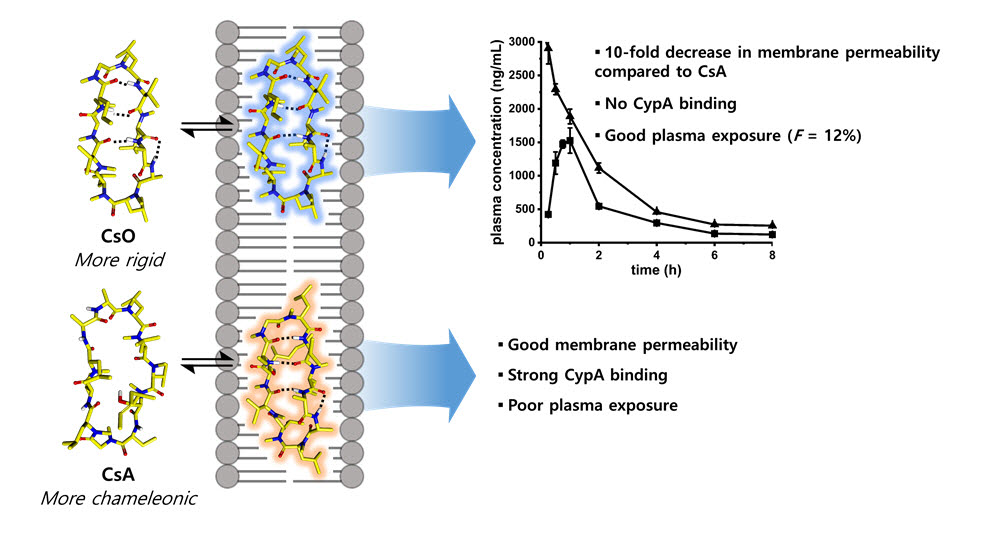

연구팀은 2차원 핵자기공명 분광기를 이용, 사이클로스포린 A와 사이클로스포린 O가 세포막의 환경과 비슷한 친유성 조건에서는 유사한 구조를 갖지만 친수성 조건에서는 다른 구조를 갖는 것을 확인했다. 이 차이가 고리형 펩타이드의 세포막 투과성과 경구투여성에 영향을 미친다는 사실을 밝혀냈다.
고리형 펩타이드의 카멜레온성 조절로 세포막 투과성과 경구투여율이 개선된 신약개발 연구 활성화에 기여할 것으로 기대하고 있다.
서지원 교수는 “중분자 신약개발에서 중요한 분자 플랫폼인 고리형 펩타이드를 이용한 신약개발에 중요한 디자인 원리를 제시했다”고 말했다.
이번 연구는 보건복지부 보건의료기술연구개발사업, 과학기술정보통신부 중견연구자지원사업 및 지스트 GRI(GIST 연구원) 사업의 지원을 받아 이뤄졌다. 미국화학회가 발행하는 의약화학 분야 국제학술지인 '의약화학 저널' 온라인에 최근 게재됐다.
광주=김한식기자 hskim@etnews.com









