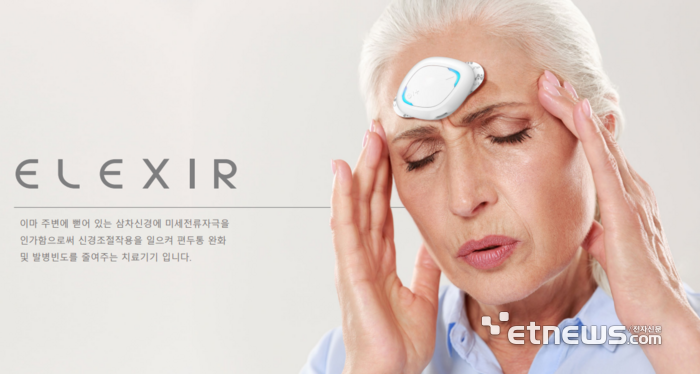
뉴아인이 전자약 파이프라인 다각화로 '전자약 대중화'를 노린다.
뉴아인은 올해 10월부터 편두통 완화기기 솔라메디(일렉시아)를 필두로 시장 공략에 나선다고 12일 밝혔다. 내년에는 주의력결핍과잉행동장애(ADHD) 치료기기 '스마일', 안구건조증 치료기 '뉴아인02'(프로젝트명) 등을 출시할 계획이다.
차세대 치료제로 불리는 전자약은 전류를 인체에 직접 자극해 치료 효과를 얻는 의료기기다. 기존 약물과 비슷한 치료 효과를 갖지만 부작용이 적은 것이 특징이다.
뉴아인은 동아제약과 일렉시아 국내 독점 판매 공급계약을 맺고, 상품명을 '솔라메디'로 변경해 10월 판매 목표로 준비 중이다. 뉴아인은 일렉시아로 연간 30억원 이상 매출을 기대하고 있다. 일렉시아는 식품의약국(FDA) 승인도 받았다.
김도형 뉴아인 대표는 “국내 편두통 유병율은 16%로 약 830만명이 편두통을 경험하고 있다”면서 “경피적 삼차신경자극으로 편두통 빈도와 통증을 완화하는 일렉시아를 국내 8000대 이상 생산해 판매할 계획”이라고 말했다.
일렉시아는 이미지 서울대병원 신경과 교수팀을 통해 8월부터 국내 추가 임상에 돌입한다.

뉴아인은 두 번째 전자약 주의력결핍과잉행동장애(ADHD) 치료기기 '스마일'을 내년 중 국내에 출시할 계획이다. 스마일 역시 미국 FDA 승인을 받았다. 스마일은 수면 중 전하 중립형 대칭 신경자극 프로토콜을 통해 ADHD 증상 완화를 유도한다. 의사 처방을 받아 7~12세 ADHD 환자 치료에 쓸 수 있다.
회사는 스마일에 탑재한 배터리 용량을 높이고, 자동충전 형태로 디자인 변경을 진행하고 있다. 미국에서 내년 1월 출시를 목표로 기기 업그레이드 중이다. 미국 FDA 허가 제품으로 국내에도 시판이 가능한지 식품의약품안전처와 논의 중이다.
세 번째 전자약인 '뉴아인02' 확증임상은 180명 대상으로 진행 중이다. 뉴아인02는 각막 손상으로 발생하는 건성안과 각막통증을 치료하는 전자약이다. 뉴아인02는 내년 1분기 내 결과 분석을 마치고 2~3분기 중 출시가 목표다.
추가로 황반변성 전자약도 개발 중이다. 지난 6월 산업통상자원부에서 공모한 '2023년 바이오산업기술개발사업 전자약 연구개발기관'으로 선정됐다. 건성 황반변성 환자를 대상으로 전하균형 망막자극 치료기술의 다기관 확증임상시험을 수행한다.
뉴아인 관계자는 “녹내장, 황반변성 환자 치료를 위한 전자약으로 손상된 시신경을 재생하는 개념으로 개발하고 임상 검증 중”이라고 말했다.
송혜영 기자 hybrid@etnews.com









