미국이 의료기기와 연동 가능한 모바일 헬스케어 애플리케이션(앱)을 공식 승인했다. 지난 2013년 모바일 헬스케어 앱 규제를 강화한 이후 2년 만이다.
워싱턴포스트 및 주요 외신은 26일 미국 식품의약국(FDA)이 의료기기 전문 업체 덱스콤이 내놓은 모바일 헬스케어 시스템 ‘덱스콤 셰어 시스템’을 공식 승인했다고 보도했다.
이미 유사한 서비스들이 있지만 FDA의 공식 승인을 받은 것은 지난 2013년 모바일 헬스케어 앱 규제 강화 이후 처음이다. 미국 모바일 헬스케어 시장이 본격적으로 개화할 움직임이라는 해석이다.
덱스콤의 모바일 헬스케어 시스템은 당뇨병 환자의 혈당 수치를 담당의사에게 실시간 전달하고 간병인이나 보호자가 원격에서 데이터를 살펴볼 수 있다. 연속혈당측정기(CGM)를 환자의 피부에 부착한 후 측정기 내부의 조그만 센서를 피부 아래 넣어 환자의 생체정보를 자동으로 모바일 앱에 공유한다. 환자용 앱과 보호자용 앱이 별도로 있고 환자가 데이터 수신자를 선택할 수 있다.
알베르토 구티에레즈 FDA 의료기기·진단보건센터(CDRH) 국장은 “당뇨병을 앓고 있는 아이를 둔 부모 등에겐 이 혁신적인 기술이 오랜 숙원이었다”며 “이번 공식 승인은 향후 비슷한 기술이 미국에 널리 퍼지는 계기가 될 것”이라고 말했다.
FDA는 이번 승인과 함께 서비스와 연계한 기기를 시판 전 승인 절차를 밟지 않고 등록만 하면 되는 ‘클래스Ⅱ’로 분류했다. 현재 비슷한 형태의 기계로 모바일 헬스케어 사업을 벌이는 업체들 역시 기기등록만 하면 팔 수 있다는 얘기다.
앞서 FDA는 지난 2013년 심장박동 수·혈압 측정 등 의학 기술이 포함된 모바일 의료 앱의 사전 승인을 강화하는 가이드라인을 발표했다. 의료 관련 앱이 환자의 생명과 건강에 큰 영향을 미친다는 판단에서다. 가이드라인에는 앱에 연결하는 기기가 적절한 승인을 받았는지, 모바일 플랫폼의 정보 전환 과정이 잘 이뤄지는지 등 플랫폼과 앱, 기기뿐 아니라 모바일 앱 제조사의 세부 내용도 명시됐다.
이번 FDA의 결정으로 미국 내 모바일 헬스케어 시장의 급성장도 예측된다.
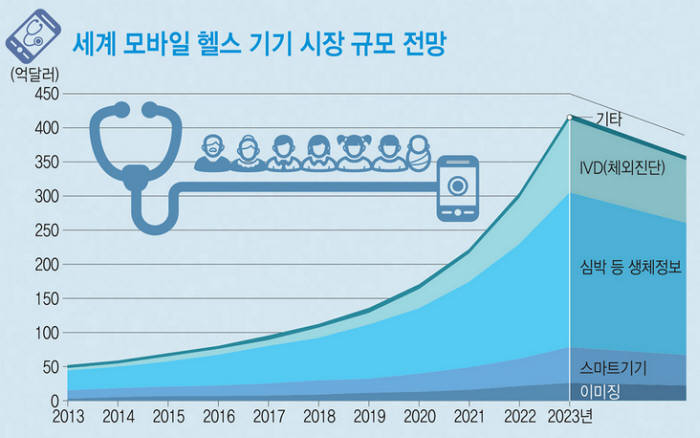
세계이동통신사업자협회(GSMA)는 최근 2017년 모바일 헬스케어 시장 격전지로 미국을 꼽고 시장 규모가 59억달러에 달할 것으로 전망했다. 모바일 의학기기 시장은 지난 2013년보다 오는 2023년 여덟 배 성장해 418억달러에 이를 것으로 시장조사업체 럭 연구소가 내다봤다. 이 중 건강상태를 모니터링하는 장치는 같은 기간 3억7200만달러 규모에서 2023년 160억달러에 이를 것으로 예측됐다.
지금까지 모바일 헬스케어 시장은 글로벌 정보통신(IT) 업계의 차세대 먹거리로 주목받았다. 애플은 지난해 모바일 운용체계(OS) ‘iOS8’를 발표하면서 모바일 헬스케어 플랫폼 ‘헬스키트’를 기본 탑재하고 스마트워치 ‘애플워치’의 핵심으로 헬스케어 기능을 꼽았다. 구글도 지난해 연례 개발자콘퍼런스에서 헬스케어 플랫폼 ‘구글핏’을 공개하고 삼성전자도 헬스케어 플랫폼 ‘사미’를 선보인 바 있다.
하지만 모바일 헬스케어 선진국으로 알려진 미국에서도 당국의 규제 탓에 시장 확대에 한계가 있었다. 대부분 실용성이 높은 부착·침습형이 아닌 착용형(웨어러블) 기기와 연계한 모바일 시스템을 내놓거나 의료기관과 연계하지 않는 일상생활에서의 웰니스 서비스를 제공하는 데 그쳤다.
김주연기자 pillar@etnews.com







