보건복지부는 식품의약품안전처는 서울대병원이 신청한 임상연구 계획이 '고위험 첨단재생의료 임상연구'로 승인됐다고 8일 밝혔다. 지난해 9월부터 시행한 '첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법령'에 따른 첫 승인 사례다.
강영진 서울대병원 소아청소년과 교수팀이 신청한 이번 임상연구는 CAR-T를 사용한 소아청소년 급성 림프모구백혈병 환자 치료가 목적이다.
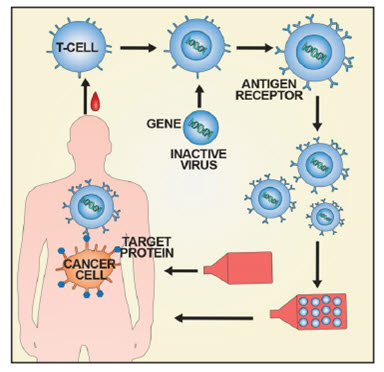
CAR-T는 면역세포(T세포) 수용체 부위와 암세포 표면 특징적인 항원 인식 부위를 융합한 유전자를 환자 T세포에 도입한 것이다. 암세포 표면 항원을 인지해 공격하는 기능을 갖는다.
고위험 첨단재생의료 임상연구는 '사람의 생명 및 건강에 미치는 영향이 불확실하거나 그 위험도가 큰' 연구다. 획기적 방법으로 희귀난치질환자 치료가 가능하나 위험도가 높은 만큼 안전성과 유효성에 대한 세밀한 심사가 요구된다.
소아청소년 급성림프모구백혈병 환자들은 그동안 항암화학요법 등 치료를 받아왔으나, 재발성·불응성 환자는 기존 치료로 백혈병 세포가 감소하지 않아 한계가 있었다.
CAR-T를 사용한 치료는 암세포만을 정확히 표적으로 삼으면서 체내 정상 세포 손상을 최소화하여 치료의 효과도 높이며, 기존 치료 부작용도 최소화할 것으로 기대된다.
김영학 보건복지부 재생의료정책과장은 “고위험 임상연구 1호 승인 이후 다양한 희귀난치질환에 대한 임상연구를 통해 희귀난치질환자들의 치료 기회를 제고할 것”이라면서 “임상연구 결과를 토대로 추후 많은 환자들에게 제공될 수 있는 치료제가 개발되기를 기대한다”고 말했다.
김시소기자 siso@etnews.com









