한국과학기술원(KAIST·총장 이광형)은 김윤기 생명과학과 교수팀이 진핵세포 내에서 일어나는 원형 RNA(circular RNA) 단백질 합성 과정에 대한 새로운 메커니즘을 규명했다고 23일 밝혔다.
현재 널리 사용되는 코로나바이러스 mRNA 백신은 선형 형태 mRNA를 가지고 있어 세포 내에서 매우 불안정하다.
항체 생성 효율을 높이기 위해서 부득이 고용량의 mRNA를 접종하고 있는 상황이다. 이러한 고용량 접종은 mRNA에 기인하는 많은 부작용을 초래할 수 있다.
반면 원형 형태의 RNA는 선형 RNA에 비해 매우 안정되기 때문에 수많은 국내외 제약회사에서 RNA 안정성을 높이기 위해 원형 RNA를 개발하고 있는 상황이다. 이에 원형 RNA에서 일어나는 단백질 합성 과정에 대한 연구가 필요한 실정이다.
연구팀은 원형 RNA에서 일어나는 새로운 형태의 단백질 번역 과정을 규명했다.
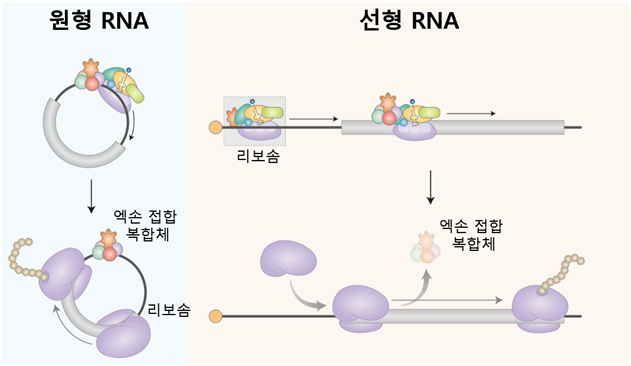
세포내에서 생성되는 대부분의 원형 RNA는 엑손 접합 복합체 (EJC)를 가지고 있음을 밝혔다. 엑손 접합 복합체는 단백질 합성을 담당하는 리보솜을 끌어오는 기능을 수행하는 단백질(eIF3g)과 직접 결합함으로써, 최종적으로 리보솜을 끌어와 단백질 합성을 유도함을 규명했다.
연구를 주도한 김윤기 교수는 “이번 연구는 안정성이 높은 원형 RNA에서 일어나는 합성 과정을 규명한 데에 연구의 의의가 있으며, 이 작용과정을 이용하여 부작용을 최소화하고, 고안정성 및 고효율 단백질 합성이 가능한 mRNA 백신을 개발할 수 있을 것으로 기대하고 있다”며 소감을 밝혔다.
특히 원형 RNA 기술 상용화를 위해 김윤기 교수는 라이보텍 벤처회사의 공동대표를 맡고 있다.
KAIST 생명과학과 장지윤, 신민경 박사과정생, 박주리 박사가 공동 제1 저자로 참여한 이번 연구는 세계 최고 수준의 국제 학술지 '핵산 연구 저널지(Nucleic Acids Research)'에 10월 9일 자로 소개됐다.
김영준 기자 kyj85@etnews.com









