암 치료 방법은 크게 수술과 방사선치료, 항암요법 세 가지다. 이중 방사선치료는 건강이 안 좋아 환자가 수술을 받기 어렵거나 수술이 어려운 부위에 생긴 암을 치료할 때 시행한다. 문제는 방사선을 쪼여도 쉽게 죽지 않는 암세포가 있다는 점이다. 특히 폐암에서 방사선 치료가 어려운 경우가 많이 발생한다.
폐암은 세포조직에 따라 크게 비소세포암(큰 세포암)과 소세포암(작은 세포암)으로 나뉜다. 폐암의 70~80%가 비소세포암이고, 수술을 통해 암 세포를 절제하고 이후 방사선 치료와 항암요법을 병행하는 것이 가장 좋다. 하지만 비소세포암은 조기진단이 어렵고 방사선 치료 시 방사선에 저항성을 보이는 것으로 알려져 있다.
비소세포암의 방사선 치료에 대한 생물학적 반응은 방사선 치료의 제약을 가져오기 때문에 비소세포암 내 방사선 저항성을 유도하는 타깃 분자를 찾아내고, 이들의 분자적인 신호를 규명함으로써 폐암 치료 한계를 극복하려는 노력이 진행되고 있다.
한국원자력의학원(원장 조철구) 황상구 박사팀은 방사선을 쪼여도 잘 죽지 않는 암 세포의 유전정보를 분석해 ‘HRP-3’ 단백질이 암 치료를 저해하는 것을 확인했다. HRP-3를 제어해 방사선치료 효율을 높이는 방법도 함께 개발했다.
HRP-3 단백질은 HDGF 단백질 그룹의 하나로, 현재까지 HRP-1 부터 HRP-4까지 4개의 단백질이 밝혀졌다. HDGF 단백질은 암의 성향을 공격적으로 변화시키는 요인으로 알려져 있으나 HRP 단백질은 암과 관련된 기능이 거의 알려져 있지 않다. 특히 HRP-3 단백질의 주된 기능은 신경세포 분화에 중요한 역할을 한다고 알려져 있었으나 폐암의 방사선 치료 저항성에 대한 기능은 이번에 처음 밝혀졌다.
연구팀은 폐암의 방사선 치료 시 방사선 저항성과 HRP-3 단백질의 관련 기능을 밝혀냈다. 향후 폐암 환자 맞춤형 방사선 치료 기술 개발과 방사선 치료 예후를 예측하는데 중요한 바이오 마커가 될 것으로 기대된다.
연구를 통해 비소폐암세포가 방사선 및 항암제에 대해 서로 다른 민감도를 나타내고, 특히 폐암세포주에서 HRP-3의 양적 차이가 현저함을 밝혀냈다.
실험에서 HRP-3의 핵산 및 단백질 양이 상대적으로 많은 암세포는 방사선과 항암제 처리에 저항성을 보였다. 상대적으로 양이 적은 암세포는 동일한 처리를 했더니 세포가 사멸됐다. HRP-3의 양에 따라 방사선 치료 저항성이 달라진다는 사실이 확인된 것이다.
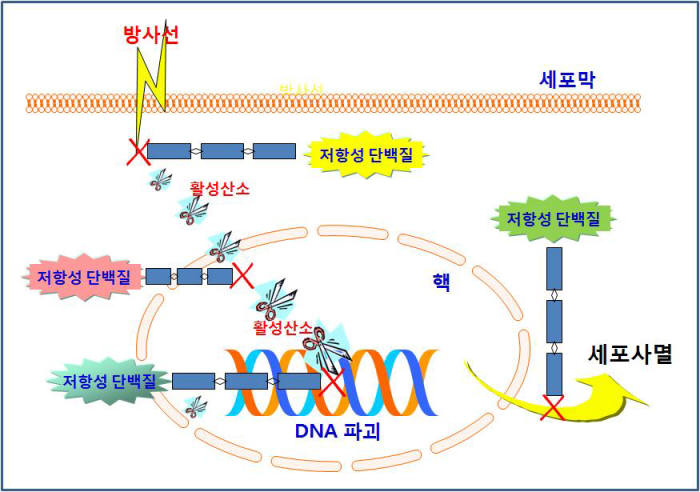
연구팀은 암세포 내에 HRP-3 유전자를 억제하면 항산화제 분자가 감소하고, 방사선에 의해 발생하는 암세포 내 활성산소를 제거하지 못하는 것을 관찰했다. 결국 세포 내 활성산소가 많아지면서 암세포 사멸이 증진되면서 방사선에 대한 민감성이 증가함을 확인했다.
이 연구를 통해 방사선 저항성 단백질의 신호전달 네트워크를 구축하고, 폐암의 방사선 저항성 핵심 분자를 타깃으로 한 암치료 신약을 개발할 수 있을 것으로 기대된다. 연구팀은 ‘폐암 환자 방사선 치료 예후 예측, 바이오 진단키트 개발’ ‘표적 암 치료 신약 개발’ 등에 적용해 5년 내에 임상활용이 가능할 것이라고 전망했다.
권건호기자 wingh1@etnews.com









