4조원 규모 미국 항암제 시장을 놓고 국산 바이오시밀러 업계 점유율 확보전이 시작된다.
삼성바이오에피스와 셀트리온은 하반기 오리지널 의약품 물질특허가 만료됨에 따라 바이오시밀러 출시 채비를 마쳤다.
지난해 말 셀트리온에 이어 삼성바이오에피스도 미국 식품의약국(FDA)으로부터 유방암·위암 치료제 '허셉틴' 바이오시밀러 판매허가를 획득했다. 유럽시장 성장세를 이어 하반기부터 미국에 진출한다.
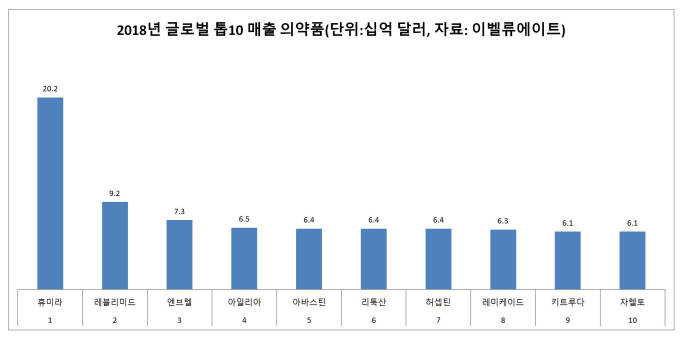
허셉틴은 위암과 전이성 유방암 치료에 사용되는 항암제다. 글로벌 제약사 로슈 자회사인 제넨텍이 개발했다. 이밸류에이트에 따르면 지난해 기준 세계 판매 매출은 7조원이 넘는다. 세계 블록버스터 의약품 중 7위에 올랐다.
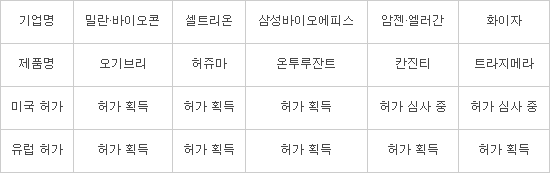
전체 7조원 중 4조원가량이 미국에서 판매된다. 세계 최대 시장이다. 미국에서는 밀란·바이오콘이 지난해 12월 '오기브리'를 허셉틴 바이오시밀러로는 최초로 FDA 허가를 받았다. 셀트리온 '허쥬마'가 뒤를 이었다. 최근 허가를 받은 삼성바이오에피스 '온투루잔트'까지 포함하면 세 개 제품이 미국 진출 준비를 마쳤다. 암젠·엘러간(칸진티), 화이자(트라지메라)까지 연내 허가가 유력해 4조 미국 시장을 둘러싼 경쟁이 치열해질 전망이다.

판매는 6월 이후가 유력하다. 오리지널의약품 '허셉틴' 물질특허는 6월 만료된다. 기술특허 등 기타 특허가 남아있어 오리지널 의약품 기업 소송 가능성이 있다. 위험을 감수하고 선제 출시 가능성도 배제 못하지만, 3분기 이후가 유력하다.
삼성바이오에피스 관계자는 “최근까지 물질특허 만료와 동시에 바이오시밀러를 출시한 사례가 있지만, 소송과 판매를 동시에 끌고 가기에 부담이 있다”면서 “내부 출시 일을 논의 중인데, 6월 이후가 될 가능성이 높다”고 말했다.
자가면역질환 치료용 바이오시밀러 시장을 주도하는 셀트리온과 삼성바이오에피스가 항암제 시장에서 맞붙는다. 유럽에서는 작년부터 경쟁을 시작했다.
삼성바이오에피스 '온투루잔트'는 2017년 9월 허셉틴 바이오시밀러로는 처음으로 유럽 허가를 받았다. 셀트리온도 뒤이어 작년 2월 '허쥬마' 허가를 획득했다. 성장세는 셀트리온이 조금 앞선다. 지난해 허쥬마는 유럽시장에서 약 6% 점유율을 확보한 것으로 알려졌다. 암젠, 삼성바이오에피스 등이 3~5% 점유율을 기록하며 뒤를 잇는다. 유럽 의약품시장이 조달입찰이 대부분인 것을 감안, 대형병원 입찰 한 두 개면 순위가 언제든지 바뀐다.
항암 바이오시밀러 시장 마케팅이 성공 여부를 판가름한다. 셀트리온, 삼성바이오에피스 등 국산 바이오시밀러 기업 주력 제품은 자가면역질환 치료 영역이다. 항암제와 비교해 단가가 낮고, 가격이 제품 선택 필수요소는 아니다. 상대적으로 바이오시밀러에 보수적인 데다 조달이 아닌 개별병원 영업이 관건인 미국 시장에서 새로운 전략이 요구된다.
셀트리온헬스케어 관계자는 “허쥬마는 지난해 기준 유럽 출시 3개월 만에 의미 있는 점유율을 확보하면서 첫 제품인 램시마 성장 속도를 넘어섰다”면서 “현지 맞춤형 마케팅 전략으로 주력 제품으로 키울 것”이라고 말했다.
<허셉틴 바이오시밀러 현황(자료: 업계 취합)>
[전자신문 CIOBIZ] 정용철 의료/바이오 전문기자 jungyc@etnews.com